
专升本社区是一家为广大升本学子提供全国专升本政策,考试大纲,备考信息,报名考试时间,考试科目,复习资料,升本专业,升本院校等信息的资讯类网站。本网站为了保护网络信息安全,保障用户合法权益的同时为广大学员提供更优质的服务,将严格遵循合法、正当、必要的原则,收集您的个人信息和需求。承诺在本网站中收集到的您个人信息将受到严格的保护,为了使您能得到优质的服务,仅限于向专升本社区网站总部及您所在地区分校教务人员提供您的个人信息(包括姓名、联系电话、就读院校),并承诺将严格保护,不得向任何第三方泄露或披露,并确保不对您造成骚扰。 如您选择线上咨询平台上的升本在线服务,即表示您完全知晓并同意上述专升本社区网站收集、使用信息的目的和方式和范围,请填写您的个人信息;如您不同意,您可选择退出本网页,选择其他方式了解升本在线服务。
本网站收集、使用用户信息规则:
1、本网站收集用户信息仅限于结合教育考试院政策,根据所在地区不同,为用户提供高效优质的服务。
2、本网站工作人员对在业务活动中收集的公民个人信息将严格保密,不向与本机构无关的任何他人提供用户的个人信息。
3、本网站已经并将采取最新的技术措施和其他必要措施,确保信息安全,防止在业务活动中收集的公民个人电子信息泄露、毁损、丢失。
4、本网站加强对机构工作人员对个人信息使用权限的管理,发现违规泄露、散布用户个人信息的,将立即停止传播该信息,并对工作人员按规定进行处罚。
5、用户如发现泄露个人身份、散布个人隐私等侵害其合法权益的网络信息,有权要求本机构删除有关信息或者采取其他必要措施予以制止。
免责声明:
1、本网站所刊载的各类形式(包括但不仅限于文字、图片、图表)的作品仅限于为广大学员提供更多信息及更优质的服务,仅供用户参考。对于访问者根据本网站提供的信息所做出的一切行为,除非另有明确的书面承诺文件,否则本网站不承担任何形式的责任。
2、本网站及其雇员一概无需以任何方式就任何信息传递或传送的失误、不准确或错误对用户或任何其他人士负任何直接或间接的责任。
3、凡以任何方式登录本网站或直接、间接使用本网站资料者,视为自愿接受本网站声明的约束。
4、本网站若无意中侵犯了哪个媒体或个人的知识产权,请致函或来电告之,本网站将立即给予删除等相关处理,全国统一来电400-023-1785;全国统一邮箱kf@hlsjy.com。
5、以上声明内容的最终解释权归专升本社区网站所有。

感谢您信任并使用专升本社区的服务!我们根据最新的法律法规、监管政策要求,更新了《用户隐私政策》。 本次更新进一步明确了我们如何收集和使用您的信息以及如何存储您的信息。请您仔细阅读并充分理解以下条款,特别提醒您应留意本《用户隐私政策》中加粗形式的条款内容。如果您不同意本《用户隐私政策》,您可能无法正常使用我们的产品、服务。
希望您仔细阅读并充分理解本《用户隐私政策》,了解在使用我们的产品和服务时,我们如何收集、使用、存储、处理和保护这些信息,以及我们为您提供的了解、控制这些信息的方式,以便您更好地了解我们的产品和服务并作出适当地选择。
如您使用或继续使用我们的产品和服务,表示您同意或/和已征得您的父母或监护人的同意(若您为未成年人)按照本《用户隐私政策》收集、使用、储存、处理和保护您的信息。
本《用户隐私政策》主要向您说明如下信息:
1. 我们如何收集和使用您的信息
2. 我们如何存储您的信息
3. 我们如何使用Cookie以及同类技术
4. 我们可能向您发送的信息
5. 您如何了解和控制自己的用户信息
6. 我们如何保护您的个人信息
7. 本《用户隐私政策》的适用范围
8. 本《用户隐私政策》如何更新
9. 如何与我们联系
1. 我们如何收集和使用您的信息
1.1 我们将根据合法、正当、必要的原则,按照如下方式收集您在使用服务时主动提供的或因为使用服务而产生的信息,用以向您提供服务、优化我们的服务以及保障您的帐户安全。
1.2 您在注册、登录时提供的个人信息及我们的使用方式:
(1) 如您用其他方式注册、登录专升本社区相关产品时,我们会收集手机号码、密码。如您仅需浏览、搜索等功能,您不需要注册或登录,亦无需提供以上信息。如您不提供手机号码,将无法使用我们的服务。
(2) 如您以第三方帐号(如微信等帐号)登录专升本社区相关产品时,我们会收集您第三方帐号的个人信息(包括头像、昵称及您提供的其他信息),您可以在关联登录页面选择是否授权或新建个人信息。 我们和第三方将以去标识化的方式验证,这个过程中我们收集到的验证信息除前述头像、昵称及您提供其他信息外,无法识别特定个人身份的信息。我们需要您确认通过第三方帐号登录前已经在第三方完成实名认证。如您不同意第三方帐号登录,将无法使用第三方帐号登录验证功能,但不影响您使用我们的其他服务。
(3) 我们收集手机号码、微信等帐号是用于为您提供帐号登录服务以及保障您的帐号安全。
1.3 您在产品或服务中主动提供的信息及我们的使用方式:
(1) 如您在个人资料编辑时提供的昵称、头像、性别、学校、地区、报考城市、考试类型、真实姓名、电子邮件、个人简介。这些资料将帮助我们更好地了解您并为您提供更优质的服务。
(2) 如您使用观看视频、直播、试题纠错、使用反馈、课程分享、学习笔记时,我们会收集您通过前述服务所上传或下载的信息,这类信息包括搜索关键字、发布和回复的评论、文字、标签。
(3) 如您使用客服等用户响应功能时,您可能需要提供您的手机号码、QQ号码或您向我们主动提供的其他联系方式,我们收集这些信息是为了核验您的用户身份信息、调查事实、帮助您解决问题,如您拒绝提供可能导致您无法使用我们的客服等用户响应功能。我们亦会保存您与我们的客服沟通信息和回复内容。
1.4 我们在您使用我们的产品和服务时获取的信息及我们的使用方式:
1.4.1 为保障您正常使用我们的产品和服务,维护我们产品和服务的正常运行,改善及优化您的服务体验并保障您的帐号安全,我们会收集您的下述信息:
(1) 日志信息:当您使用我们的产品和服务时,我们可能会自动收集相关信息并存储为服务日志信息。如登录帐号、IP地址、搜索记录、收听观看记录、网页浏览记录、服务故障信息等。
1.5 我们会根据以上在您使用产品或服务时获取的信息开展数据分析和研究,改进我们的内容布局和推广效果,为商业决策提供产品或服务支持。
1.6 其他用户分享的信息中含有您的信息及我们的使用方式
如其他用户发布的笔记、回复中可能包含您的信息。我们将无法修改其他用户的信息,如实展示可能包含您的信息。如您认为侵犯您的个人信息,请您通过下述第11条投诉方式和联系方式联系我们进行处理。
1.7 请您理解,我们向您提供的功能和服务是不断更新和发展的,如果某一功能或服务未在前述说明中且收集了您的个人信息,我们会通过页面提示、交互流程、网站公告等方式另行向您说明信息收集的内容、范围和目的,以征得您的同意。
1.8 关于个人信息和个人敏感的提示
上述的个人信息和个人敏感信息,我们会尽最大努力保护您的信息,若您不提供该信息,您可能无法正常使用我们的相关服务,但不影响您使用服务中的其他功能。若您主动提供您的个人信息和个人敏感信息,即表示您同意我们按本《隐私政策》所述目的和方式使用您的个人信息和个人敏感信息。
2. 我们如何存储您的信息
2.1 存储信息的地点
我们遵守法律法规的规定,将境内收集的用户个人信息存储于境内。目前我们不会跨境传输或存储您的个人信息。将来如需跨境传输或存储的,我们会向您告知信息出境的目的、接收方、安全保证措施和安全风险,并征得您的同意。
2.2 存储信息的期限
一般而言,我们仅为实现目的所必需的最短时间内或法律法规规定的条件下存储您的个人信息,并在超出个人信息保存期限后对您的个人信息进行删除或匿名化处理。但在下列情况下,我们有可能在遵守法律法规规定的前提下,更改个人信息的存储时间:
(1) 为遵守相关法律法规的规定;
(2) 为遵守法院判决、裁定或其他法律程序的规定;
(3) 为遵守相关政府机关或法定授权组织的要求;
(4) 为执行相关服务协议或本《隐私政策》、维护社会公共利益,为保护们的客户、我们或我们的关联公司、其他用户或雇员的人身财产安全或其他合法权益所合理必需的用途。
(5) 其他法律法规规定或您另行授权同意的情形。
2.3 存储信息的方式
我们会通过安全技术保护措施存储您的信息,包括本地存储、数据缓存、数据库和服务器日志。
2.4 当我们的产品或服务发生停止运营的情形时,我们将采取合适的方式(例如推送通知、站内信、公告等形式)通知您,并在合理的期限内删除或匿名化处理您的个人信息。
3. 我们如何使用Cookie以及同类技术
Cookie 和同类技术是互联网中普遍使用的技术。当您使用专升本社区及相关服务时,我们可能会使用相关技术收集您的信息。我们使用 Cookie 和同类技术主要为了实现以下功能或服务:
3.1 保障产品与服务的安全、高效运转:我们可能会设置认证与保障安全性的 Cookie 或匿名标识符,使我们确认您是否安全登录服务,或者是否遇到盗用、欺诈及其他不法行为。这些技术还会帮助我们改进服务效率,提升登录和响应速度。
3.2 帮助您获得更轻松的访问体验:使用此类技术可以帮助您省去重复您填写个人信息、输入搜索内容的步骤和流程(例如:表单填写)。
您可以通过浏览器设置拒绝或管理Cookie以及同类技术的使用。但请注意,如果停用Cookie,您可能无法享受最佳的服务体验,某些服务也可能无法正常使用。
4. 我们可能向您发送的信息
4.1 信息推送
您在使用我们的产品和服务时,我们可能向您发送提醒、声音和图标标记,以及电子邮件、短信等其他方式的推送通知。 您可以在设备的设置等相关页面选择取消。
4.2 与产品和服务有关的公告
我们可能在必要时向您发出与产品和服务有关的公告。 您可能无法取消这些与产品和服务有关、性质不属于广告的公告。
5. 您如何了解和控制自己的用户信息
5.1 我们将尽一切可能采取适当的技术手段,保证您可以了解、更新和更正自己的注册信息或使用我们的服务时提供的其他用户信息。在了解、更新、更正和删除前述信息时,我们可能会要求您进行身份验证,以保障帐户安全。一般情况下,您可随时修改自己提交的信息,但出于安全性和身份识别的考虑,您可能无法修改注册时提供的某些初始注册信息、验证信息及认证信息。
5.2 如您不希望您的部分信息被我们获取,您可以通过关闭设备权限的方式停止我们获得您的个人信息。您开启下述权限即代表您授权我们可以收集和使用该权限相应的个人信息来为您提供对应服务,您关闭前述权限即代表您取消了授权,我们将不再基于对应权限继续收集和使用相关个人信息,也无法为您提供该权限所对应的服务,但不影响您使用我们的其他服务。但是,您关闭权限的决定不会影响我们此前基于您的授权所进行的信息收集及使用,但您可以通过第5.3条内容删除有关记录:
5.3 在您使用专升本社区期间,为了让您更便捷地控制您的个人信息,我们在产品和服务设计中为您提供了相应的操作设置,您可参考下面的指引进行操作。
5.3.1 访问个人信息:
您可以在【个人主页】-【头像】-【编辑资料】进行查询、访问、更正您的头像、昵称、性别、生日、地区、个性签名、兴趣爱好。
6. 我们如何保护您的个人信息
6.1 为保障您的个人信息安全,我们在合理的安全水平内使用各种安全保护措施来保障您的信息,防止数据遭到未经授权访问、公开披露、使用、修改、损坏或丢失。例如,我们使用加密技术(如SSL)、匿名化处理等手段来保护您的个人信息。
6.2 我们建立专门的管理制度、审批流程和组织确保信息安全。例如,我们严格限制访问信息的人员范围,要求他们遵守保密义务,并进行审查。
6.3 我们鼓励我们的工作人员学习信息安全知识、提高个人信息安全保护意识,并定期或不定期对我们的工作人员进行信息安全培训。
6.4 若不幸发生个人信息泄露等安全事件,按照法律法规要求,我们会启动应急预案,阻止安全事件扩大,并及时告知您:安全事件的基本情况和可能的影响、我们已采取或将要采取的处置措施、您可自主防范和降低风险的建议、对您的补救措施等。我们将及时将事件相关情况以邮件、信函、电话、推送通知等方式告知您,难以逐一告知用户时,我们会采取合理、有效的方式发布公告。同时,我们还将按照监管部门要求,主动上报个人信息安全事件的处置情况。
6.5 互联网环境并非百分之百安全,当出现下列非因我们过错而对您的信息造成泄露及由此造成的损害结果,我们无需承担任何责任:
(1) 任何由于黑客攻击、计算机病毒侵入或发作、因政府管制而造成的暂时性关闭等影响网络正常经营之不可抗力而造成的个人资料泄露、丢失、被盗用或被篡改等。
(2) 在使用专升本社区的过程中链接到其它网站或因接受来自第三方的服务所造成之个人资料泄露及由此而导致的任何法律争议和后果。
(3)如您在使用专升本社区(例如笔记、评论等)的过程中主动公开、上传、发布或向第三方提供您的个人信息的,其他用户可能会收集您的个人信息。
7. 本《用户隐私政策》的适用范围
7.1 我们的所有产品和服务均适用本《用户隐私政策》。但某些产品或服务可能会有其特定的隐私政策适用条款,该特定隐私政策适用条款更具体地说明我们在该产品或服务中如何处理您的个人信息。除非有特殊说明,若本《用户隐私政策》与该特定产品或服务的隐私政策适用条款有不一致之处,请以该特定隐私政策适用条款为准。
7.2 请您注意,本《用户隐私政策》不适用由其他公司或个人提供的产品或服务。如果您使用第三方的产品或服务,须受该第三方的隐私政策而非本《用户隐私政策》)约束,您需要仔细阅读其政策内容。
7.3 本《用户隐私政策》为《用户服务协议》及相关协议的重要组成部分,本《用户隐私政策》内的名词定义参照《用户用户服务协议》,适用于专升本社区相关服务。
8. 本《用户隐私政策》如何更新
8.1 随着我们的服务范围扩大,我们可能适时更新本《用户隐私政策》的条款,更新内容构成本《用户隐私政策》的一部分。如更新后的《用户隐私政策》导致您的权利发生实质改变,我们将在更新前通过显著位置提示或以其他方式通知您,为避免您不能及时获知更新,请您经常阅读本《用户隐私政策》。
8.2 无论何种方式,若您继续使用我们的服务,即表示同意受更新后的《用户隐私政策》约束。
8.3 更新后的《用户隐私政策》将以更新日期为生效日期,并取代之前的《用户隐私政策》。
9. 如何与我们联系
若您对本《用户隐私政策》有问题、意见、建议,或者与用户个人信息安全相关的投诉、举报,您可以通过全国统一来电400-023-1785;全国统一邮箱kf@hlsjy.com等方式与我们进行联系,我们将在收到函件并验证您的用户身份后尽快予以回复。

 我要收藏
我要收藏
考试大纲大家都知道其重要性,因为考试的题型基本来源于考试大纲中,为了帮助到大家安心备考,以下是来源于网上,由江西专升本社区整理出的2021年上饶师范学院专升本考试《普通化学》考试大纲。
上饶师范学院普通高校专升本招生统一考试《普通化学》试题,主要考查学生的基础知识与基本技能,以及运用所学普通化学知识和方法分析问题和解决问题的能力。
本科考试时间为120 分钟,总分为 150 分。
一、考试范围及要求
(一)参考书目
1.《无机化学》,编著者:吉林大学、武汉大学、南开大学,高等教育出版社 ,2019年1月第四版
2.《无机化学》,编著者:武汉大学、吉林大学等,高等教育出版社 ,1994年4月第三版
3.《无机化学》,编著者:北京师范大学、华中师范大学等,高等教育出版社,2003年1月第四版。
(二)课程内容与考核要求
1.物质状态
(1)知识点:理想气体状态方程,分压定律,液体的蒸发,沸点。
(2)考核要求:理想气体状态方程,分压定律的内容与应用
2. 原子结构
(1)知识点:几率密度和电子云,波函数的空间图象,四个量子数,多电子原子的能级,核外电子排布的原则及其与元素周期表的关系,元素基本性质的周期性。
(2)考核要求:四个量子数,多电子原子的能级,核外电子排布的原则,元素基本性质的周期性。
3. 化学键与分子结构
(1)知识点:离子键的本质与特特征,离子晶体,共价键的本质和特点,杂化轨道理论,价层电子对互斥理论,分子轨道理论,键参数与分子的性质,分子晶体和原子晶体,极性分子和非极性分子,分子间作用力,离子的极化。
(2)考核要求:杂化轨道类型,价层电子对互斥理论判断分子的构型,分子的极性及其间的作用力。
4. 氢和稀有气体
(1)知识点:氢的成键特征,氢的性质、制备方法,氢的化合物,氙的性质及其氟化合物的空间结构与性质。
(2)考核要求:氢键、氢气的实验室制备,
5. 化学热力学初步
(1)知识点:热力学基本概念,热力学第一定律,可逆途径;化学反应的热效应,盖斯定律,生成热与燃烧热,状态函数熵和吉布斯自由能,吉布斯自由能变对反应方向的影响。
(2)考核要求:热力学第一定律,吉布斯自由能变对反应方向的影响。
6. 化学反应速率
(1)知识点:反应速率理论,反应速率的影响因素。
(2)考核要求:反应速率的影响因素。
7. 化学平衡
(1)知识点:平衡常数,标准平衡常数Kθ与△rGmθ的关系,化学平衡移动的影响因素。
(2)考核要求:标准平衡常数Kθ与△rGmθ的关系,化学平衡移动影响因素。
8. 溶液
(1)知识点:溶液浓度的表示方法,溶解度原理和分配定律;非电解质稀溶液的依数性;分散体系和溶胶的性质与其粒子结构,及溶胶的聚沉和稳定性。
(2)考核要求:非电解质稀溶液的依数性,溶胶的三大性质。
9. 电解质溶液
(1)知识点:酸碱理论,强电解质溶液理论,弱酸、弱碱的解离平衡和盐的水解,缓冲溶液,难溶性强电解质的沉淀溶解平衡。
(2)考核要求:弱酸、弱碱的解离平衡,缓冲溶液PH值的计算,难溶性强电解质的沉淀溶解平衡。
10. 氧化还原反应
(1)知识点:氧化数、氧化剂还原剂等的基本概念,氧化还原反应方程式的配平,原电池和电极电势,能斯特方程,电池电动势与化学反应吉布斯自由能的关系,电极电势的应用。
(2)考核要求:氧化数、氧化还原反应方程式的配平,能斯特方程。
11. 卤素
(1)知识点:卤素的通性,卤素单质及其化合物性质,含氧酸的氧化还原性, 元素电势图。
(2)考核要求:卤素单质和含氧酸的氧化还原性, 元素电势图,。
12. 氧族元素
(1)知识点:氧族元素的通性,氧,臭氧,水,过氧化氢,硫及其化合物,无机酸强度的变化规律。
(2)考核要求:氧、臭氧、过氧化氢的结构、性质和用途,硫的氧化态所形成的重要物种的结构、性质、制备和用途,无机酸的强弱。
13. 氮族元素
(1)知识点:氮族元素的通性,氮及其化合物,磷及其化合物,砷、锑、铋及其化合物,盐类的热分解。
(2)考核要求:氮和磷的单质及其氢化物、卤化物、氧化物,含氧酸及其盐的结构、性质、制备和应用。
14. 碳族元素
(1)知识点:碳族元素的通性,碳族元素的单质及其化合物,无机化合物的水解性
(2)考核要求: C、Si的氧化物性质和结构,锡铅不同氧化态转化关系。
15. 硼族元素
(1)知识点:硼族元素的通性,硼族元素的单质及其化合物,惰性电子对效应和周期表中的斜线关系。
(2)考核要求:三氟化硼,B2H6的结构及特性,硼酸的特性,铝及其氢氧化物的两性。
16. 碱金属和碱土金属
(1)知识点:碱金属和碱土金属的通性,碱金属和碱土金属的单质及其化合物的性质,离子晶体盐类的水解性。
(2)考核要求:碱金属和碱土金属单质的性质,碱金属和碱土金属氢氧化物碱性和溶解性的变化规律。
17. 铜、锌副族
(1)知识点:锌族元素、铜族元素的通性、单质及其化合物的性质,IB族与IA族元素和IIB族与IIA族元素性质对比,
(2)考核要求:锌族,铜族单质及其化合物的性质,Cu(Ⅰ)、Cu(Ⅱ)、Hg(Ⅰ)、Hg(Ⅱ)之间的相互转化。
18. 配位化合物
(1)知识点:配位化合物的基本概念,配位化合物的组成;配位化合物的类型;配位化合物的命名;配位化合物的空间结构及几何异构现象,配位化合物的稳定性。
(2)考核要求:配位化合物的基本概念,配位化合物的组成,配位化合物的命名;
19. 过渡金属
(1)知识点:钛、钒、铬、锰各分族元素及其重要化合物的性质,Fe、Co、Ni的单质及其重要化合物的性质和用途。
(2)考核要求:元素Ti的单质性质和用途, Cr、Mn重要化合物的性质,Fe、Co、Ni的单质原子结构特征及其重要化合物的性质和用途,过渡元素的价电子构型特点。
20. 镧系及锕系元素
(1)知识点:镧系元素的通性、镧系金属、镧系元素的重要化合物;稀土元素的分布、稀土元素的分离、稀土金属配合物、稀土元素及其化合物的应用;锕系元素的通性、锕系金属、钍及其化合物、铀及其化合物 。
(2)考核要求:镧系和锕系元素的价电子构型与元素性质的关系,镧系收缩的实质及其对镧系化合物性质的影响。
二、考试形式与试卷结构
(一) 考试形式
闭卷笔试。
(二) 试卷结构
试卷包括六大题:单选题(每小题3分,15小题,共45分)、多选题(每小题5分,5小题,共25分)、判断题(每小题3分,10小题,共30分)、完成反应式(每小题2分,5小题,共10分)、简答题(每小题10分,3小题,共30分)、计算题(每小题10分,1小题,共10分),总分150分。
(三)命题原则
题力求覆盖教材主要内容,保持稳定的难易程度,着重考查学生对问题的观察、分析和综合思维的能力。要求学生熟练掌握元素周期律、物质结构、化学热力学、化学动力学、配位化学、基础电化学、和氧化还原等理论,理解和掌握重要元素化合物的基本性质、反应、制备、结构和用途。命题紧扣教学大纲的基本要求,不局限于课本中的问题,有利于现行教学与选拔人才。
(四)试题难易比例
试题不超出教材所学知识,难易度与教材相当。其中,较容易题约占40%,中等难度题约占50%,较难题约占10%。
三、样题示例
一、选择题(每小题3分,共45分)
1. 下列电子各套量子数中可能存在的是: ( C )
A.(3、0、-1、+1/2) B.(1、0、0、0) C.(3、2、0、-1/2) D.(2、-1、0、+1/2)
2.下列各组物种中,属于等电子体的是:( C )
A.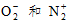 B.
B. C.CO 和 N2D.CO 和 O2
C.CO 和 N2D.CO 和 O2
3.将难挥发的非电解质溶于溶剂后,将会引起: ( A )
A. 蒸气压下降 B. 凝固点升高 C. 渗透压下降 D. 沸点下降
4. 等温等压条件下,化学反应方向的判断依据是: ( D )
A. △U B. △SC. △H D. △G
5. H2PO4-的共轭碱是: ( B )
A.H3PO4B.HPO42-C.PO43- D.OH-
6. 已知反应NO(g)+CO(g) → N2(g)+CO2(g)的
N2(g)+CO2(g)的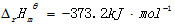 。有利于有毒气体NO和CO转化率增大的措施是:( B)
。有利于有毒气体NO和CO转化率增大的措施是:( B)
A.低温低压 B.低温高压 C.高温高压 D.高温低压
7. 下列浓度相同的溶液中,pH值最低的是: ( A )
A.NH4Cl B.NaCl C.NaOH D.NaAc
8. 下列氢氧化物没有两性的是: ( D )
A.Zn(OH)2B.Be(OH)2C.Cu(OH)2D.Fe(OH)3
9. 下列物质氧化性比较错误的是: ( A )
A.BrO3 -<ClO3 -<IO3 - B.F2>Cl2>Br2>I2
C.ClO->BrO->IO- D.HClO4<HClO3<HClO2<HClO
10.下列四类化合物中氧化能力最强的是: ( B )
A.硫酸盐 B.过硫酸盐 C.硫代硫酸盐 D.连多硫酸盐
11.下列氢化物中还原性最差的是: ( A )
A.NH3 B.PH3C.AsH3 D.SbH3
12. 下列元素中,第一电离能最小的是( B)。
A.2s22p3B.2s22p4C.2s22p5D.2s22p6
13.在相同温度下扩散速率最接近H2 气扩散速率 1/3 的气体是()。
A.CO2 B.CH4C.H2O(g) D.CO
14. 设法与SCN-离子生成血红色溶液用来鉴定该离子存在的离子是:( D )
A.Cd2+B.Co2+C.Cu2+D.Fe3+
15.在下列各组离子的溶液中,加入稀HCl溶液,组内离子均能生成沉淀的是:( C )
A.Ag+,Cu2+B.Al3+,Hg22+C.Ag+,Hg22+D.Ba2+,Al3+
二、多选题(每小题5分,共25分)
16.稀溶液的依数性包括: ( ABCD )
A.蒸气压下降B.沸点升高C.凝固点降低 D.渗透压
17.下列各对溶液中,哪对能用来配制缓冲溶液( BC )
A.HCl和NaCl B.NaH2PO4和Na2HPO4C.HAc 和 NaAc D.NaOH和NH3·H2O
18. 既易溶于稀NaOH又易溶于NH3·H2O的是: ( AC )
A.Cu(OH)2 B.Ag2O C.Zn(OH)2 D.Cd(OH)2
19. 下列化合物中可以水解的是: ( ACD )
A.SiCl4B.CCl4C.BCl3D.PCl5
20. 在分子轨道理论中,原子轨道有效组成分子轨道,应遵循下列三条原则( ABD )。
A.对称性匹配原则 B.能量近似原则 C.泡利不相容原则 D.轨道最大重叠原则
三、判断题(每题3分,共30分)
21. 蒸气压下降是溶液沸点升高和凝固点下降的原因。( Ö)
22. 298K时,指定单质的生成焓等于零,所以它的标准熵也等于零。(´)
23.非自发进行的反应就是不能发生的反应。(´)
24. 可逆化学反应达平衡时,各反应物和生成物的浓度不再随时间改变。 ( Ö)
25.平衡常数是正逆反应在平衡时的常数,不管是正反应还是逆反应平衡常数相同。 (´)
26. 在反应过程中,若生成物的分子数比反应物的分子数多,△S>0。( ´)
27. 酸碱质子理论认为碱接受质子的能力越强,碱性越强,其共轭酸的酸性越弱。 ( Ö)
28. 氨水稀释一倍,溶液中[OH-]就减为原来的1/2。 ( ´)
29. BaSO4,AgCl难溶于水,水溶液导电不显著,故为弱电解质。 ( ´)
30. 标准电极电势的数值越小,其氧化型的氧化性越弱,其还原型的还原性越强。 (Ö)
四、完成并配平下列反应方程式(每小题2分,共10分)
31. PbO2 +HCl——> PbO2 +4HCl=PbCl2+Cl2↑+H2O
32. AgCl+NH3——>AgCl+2NH3=[Ag(NH3)2]++Cl-
33. MnO4-+ SO32-+ H+——>2MnO4-+ 5SO32-+ 6H+=5SO42-+2Mn2++3H2O
34. HgCl2 + NH3——>Hg2Cl2+ 2NH3= HgNH2Cl↓ + NH4Cl + Hg
35. Na2O2+CO2——>2Na2O2+2CO2=2Na2CO3+O2
五、简答题(每小题10分,共30分)
36. 试用杂化轨道理论判断下列分子的几何构型,并加以解释。
(1)NH3 (2)H2O
答: (1)NH3 N中心原子的电子对数(5+3)/2=4, N采用sp3不等性杂化,一对孤电子对,
分子几何构型:三角锥型
(2)H2O O中心原子的电子对数(5+3)/2=4, O采用sp3不等性杂化,两对孤电子对,
分子几何构型:V型或角型
37. 比较氢卤酸(HX)的酸性大小,并说明理由。
答: HF<HCl<HBr<HCl<HI HF是弱酸,HCl到HI酸性依次增强,均为强酸。
HF分子间有氢键,使得酸性减弱。HX水溶液酸性的强弱取决于溶液中H+浓度的大小,而H+浓度的大小由HX在水溶液中的解离度的大小决定,即X-对H+的吸引能力弱,则解离度大,溶液的酸性越强,反之亦然。从F-到I-增大,离子所带电荷相同,而离子半径逐渐增加,则电荷密度逐渐降低,于是X-对H+的吸引能力逐渐降低,容易解离出H+,所以酸性增强。
38.试解释下列现象:I2溶解在CCl4中得到紫色溶液,而I2在乙醚中却是红棕色。
答: CCl4为非极性溶剂,I2溶在CCl4中后仍为分子状态,显示出I2单质在蒸气时的紫颜色。而乙醚为极性溶剂,I2溶于乙醚时与溶剂间有溶剂合作用,形成的溶剂合物不再呈其单质蒸气的颜色,而呈红棕色。
五、计算题(每小题10分,共10分)
39.利用下列数据,计算反应CaCO3(s)= CaO(s)+ CO2(g)
CaCO3(s)CaO(s)CO2(g)
 kJ/mol -1206.9-635.1 -393.5
kJ/mol -1206.9-635.1 -393.5
 J/mol ·K 92.9 39.8 213.6
J/mol ·K 92.9 39.8 213.6
(1)在298K下的 ,并判断反应的自发性。
,并判断反应的自发性。
(2)在1120K下的 ,并判断反应的自发性。
,并判断反应的自发性。
(3)求该反应能自发进行的最低温度。
解:(1) =
=  (CaO)+
(CaO)+ (CO2)+
(CO2)+ (CaCO3)
(CaCO3)
=-635.1+(-393.5)+1206.9=178.3k J/mol
 =
=  (CaO )+
(CaO )+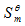 (CO2)-
(CO2)-  (CaCO3)
(CaCO3)
=39.8+213.6-92.9=160.5J/mol·K
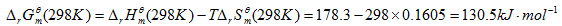 因为
因为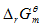 >0,所以反应在常温下是非自发的。
>0,所以反应在常温下是非自发的。
(2) 
因为 < 0, 所以反应在1120K下自发进行。
< 0, 所以反应在1120K下自发进行。
(3) 反应自发进行的最低温度为: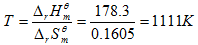
以上就是有关"2021年上饶师范学院专升本考试《普通化学》考试大纲"的全部内容了,如果你想了解更多关于江西专升本考试大纲、招生计划人数、报考政策等情况欢迎继续关注江西专升本社区(jx.zsbsq.com)!
